Entdecken Sie die Marken und Technologien unserer Unternehmensbereiche Henkel Adhesive Technologies und Henkel Consumer Brands.
12.06.2020 Düsseldorf
Henkel und Origin haben 3D-gedruckte Nasenabstrichtupfer für COVID-19-Tests entwickelt
Durch den Ausbruch der COVID-19 Pandemie hat die Nachfrage nach medizinischer Versorgung und Geräten wie Testkits zu erheblichen Lieferengpässen geführt. Um das Virus nachzuweisen, wird unter anderem ein Nasopharynx-Abstrich (NP-Abstrich) durchgeführt, bei dem Erregermaterial aus der Nasenhöhle von Patienten entnommen wird. Die notwendigen Abstrichtupfer (NP-Tupfer) werden weltweit nur von wenigen Anbietern hergestellt. In Zusammenarbeit mit Origin hat Henkel deshalb umfangreiche Materialtests auf Biokompatibilität und mechanische Widerstandsfähigkeit durchgeführt und eine Palette von 3D-druckbaren medizinischen Fotopolymeren geliefert, die für das Materialentwicklungssystem von Origin maßgeschneidert sind.
NP-Tupfer werden traditionell aus mehreren Materialien gefertigt, die vor der Sterilisation und Verpackung zusammengesetzt werden. In Zusammenarbeit mit Origin hat Henkel seine Technologieexpertise eingebracht, um NP-Tupfer zu designen, die im 3D-Druck-Verfahren massengefertigt werden können.
„Hinter unserer offenen Materialplattform stand von Anfang an die Vision, erfolgreiche Zusammenarbeit entlang der gesamten Wertschöpfungskette in der additiven Fertigung zu ermöglichen“, so Ken Kisner, Head of Innovation für den 3D-Druck bei Henkel. „In Zusammenarbeit mit Origin ist es uns gelungen, ein sehr effektives Produkt zu entwickeln. Diese medizinische Anwendung demonstriert die Möglichkeiten des 3D-Drucks weit über die Prototypenfertigung hinaus.“
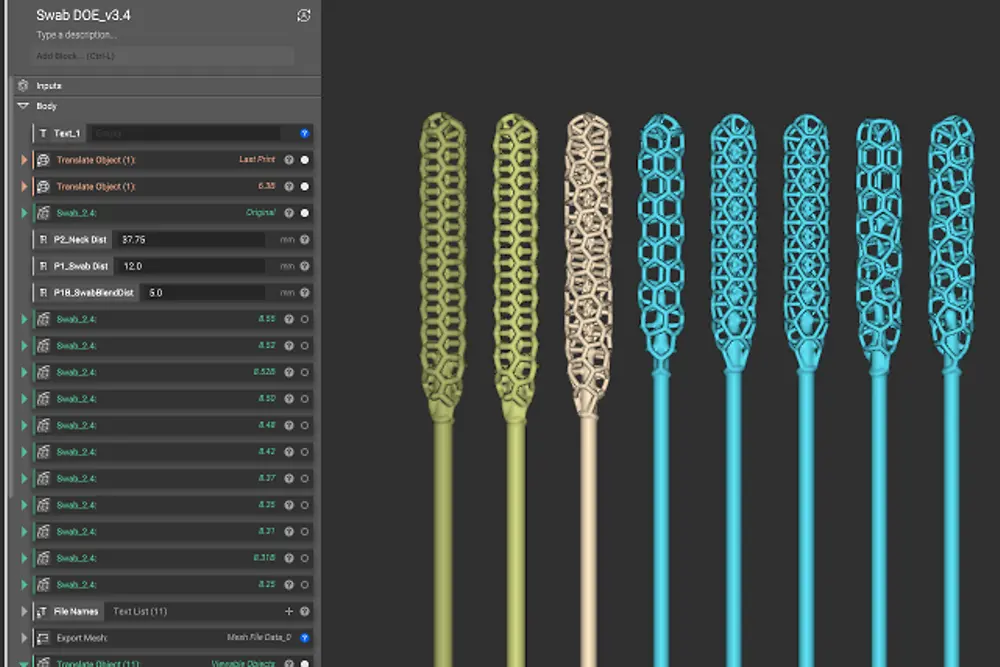
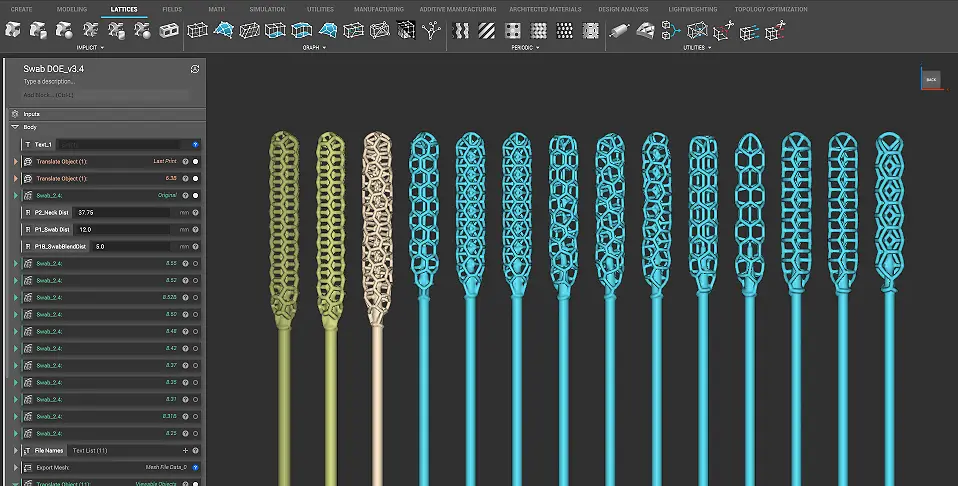
Auf Basis seiner programmierbaren Photopolymerisations-Technologie konnte Origin verschiedene Materialien, Druckparameter und Designs parallel testen und in wenigen Tagen eine optimale Lösung finden. Der finale klinisch validierte NP-Tupfer nutzt ein komplexes Gittermuster, um die Virenproben zu entnehmen. Das Design kombiniert dabei bestmöglichen Patientenkomfort mit maximaler Zuverlässigkeit.
Die Entwicklung wurde von Henkels Softwareplattform Albert unterstützt, die Innovationen durch die digitale Ermittlung einzusetzender Materialien beschleunigt. Albert hat Zugang zu sämtlichen Datensätzen rund um die breite Material- und Nachbearbeitungsexpertise von Loctite.
„Nasenabstrichtupfer sind tatsächlich sehr komplexe Instrumente“, erklärt Nick Talken, verantwortlich für die Albert Software bei Henkel. „Der Kopf des Stäbchens nutzt ein detailliertes Gittermuster, das für die maximale Entnahmemenge von Viren designt sein muss. Das gesamte Instrument muss flexibel und dabei sehr stark sein – und natürlich sicher für den medizinischen Gebrauch. Dank unserer Software Albert konnten wir sehr schnell das beste Loctite Material für diese Anwendung ermitteln.“
Origin hat bei der Entwicklung des Produktes auch mit dem Beth Israel Deaconess Medical Center (BIDMC) zusammengearbeitet, einem Lehrkrankenhaus der Harvard Medical School in Boston, Massachusetts. Das BIDMC führte eine gründliche erste klinische Untersuchung über Humanfaktoren und Materialtests durch und stellte sicher, dass das Endprodukt mit der Polymerase-Kettenreaktion, die in Laboren als Testmethode für COVID-19 angewendet wird, kompatibel ist.
„Durch die enge Zusammenarbeit und die gegenseitige Nutzung der jeweiligen Technologien haben wir einen additiven Fertigungsprozess identifiziert, optimiert und skaliert, um eine Anwendung schnellst möglich auf den Markt zu bringen“, fasst Chris Prucha, Gründer und CEO von Origin, zusammen.
Der NP-Tupfer von Origin ist als steriles Gerät klassifiziert und gilt als medizinisches Endprodukt. Das bedeutet, dass das Produkt die derzeitige “Gute Herstellungspraxis” (“current good manufacturing practices” – cGMP) einhalten muss – Vorschriften, die von der US Food and Drug Administration (FDA) durchgesetzt und im Code of Federal Regulations – Sammlung der US-amerikanischen Bundesverordnungen – dokumentiert werden. Sowohl Henkel als auch Origin haben bei der Testdurchführung und -validierung in jedem Schritt des Sterilisationsprozesses mitgearbeitet, der die Ethylenoxid-(EtO-)Sterilisation und die Autoklav-Sterilisation umfasst hat. Beide Partner haben ebenfalls mechanische Tests und eine umfangreiche Verpackungsprüfung durchgeführt und die FDA-konforme Haltbarkeit des Produktes belegt.
Darüber hinaus sind die NP-Tupfer vollständig rückverfolgbar und beinhalten einen so genannten “Digital Thread” (digitaler roter Faden), mit dem die verarbeitete Basischemie nachvollzogen werden kann. Die sterilen NP-Tupfer von Origin werden derzeit an Gesundheitseinrichtungen, Regierungsbehörden und unabhängige Testcenter in den USA und einigen weiteren Ländern ausgeliefert.
Wenn Sie mehr Informationen bekommen möchten, wie die beiden Unternehmen die 3D-gedruckten NP-Tupfer designt, entwickelt, validiert und skaliert haben, dann nehmen Sie am 26. Juni 2020 an einem Webinar mit Origin CEO Chris Prucha und Ken Kisner, Head of Innovation für den 3D-Druck bei Henkel, teil.
Zur Teilnahme können Sie sich unter folgendem Link registrieren: https://us02web.zoom.us/webinar/register/7215917432020/WN_RGk-sFk0R426KBbVYC8ZNw
Über Origin
Origin mit Sitz in San Francisco, Kalifornien, ist ein Pionier des Konzeptes der offenen Additiven Fertigung, einem neuen Weg, um auf Basis offener Materialien, erweiterbarer Software und modularer Hardware Produkte herzustellen. Origin One, der 3D-Drucker des Unternehmens für die Serienfertigung, nutzt die programmierbare Photopolymerisations-Technologie, um Licht, Hitze und Kraft neben weiteren Variablen präzise zu kontrollieren und dadurch Bauteile mit außergewöhnlicher Genauigkeit und Beständigkeit zu produzieren. Das Unternehmen arbeitet mit einem Netzwerk von Materialpartnern, um eine breite Palette kommerzieller Materialien für sein System zu entwickeln. Daraus resultieren einige der härtesten und widerstandsfähigen Materialien in der Additiven Fertigung. Das Unternehmen wurde 2015 gegründet und wird von Alumni von Google und Apple geleitet. Zu den Investoren gehören Floodgate, DCM, Mandra Capital, Haystack, Stanford University und Joe Montana. Mehr über Origin erfahren Sie hier: www.origin.io